Japan wil een kleine miljard liter met tritium verontreinigd Fukushima water lozen in de Stille Oceaan. Hoe gevaarlijk is dat?
Wat is tritium?
Tritium is een radioactieve isotoop van waterstof. Maar wat is een isotoop? Het aantal protonen in een atoomkern bepaalt hoe een atoom zich chemisch gedraagt. Alle atoomkernen met één proton in de kern gedragen zich chemisch als waterstof. Want in een neutraal atoom is het aantal protonen en aantal elektronen altijd gelijk aan elkaar. Alle chemie is in feite een wisselwerking tussen elektronen.
Alle atomen van een bepaald chemisch element hebben hetzelfde aantal protonen. Maar een atoomkern (met uitzondering van waterstof-1, dat alleen een proton heeft en nul neutronen) bevat ook neutronen. Het aantal neutronen per atoomkern van hetzelfde chemische element verschilt.
Waterstofisotoop
Deze types atoomkernen heten isotopen van het chemische element. Isotopen worden aangeduid met de naam van het chemische elementen, met daarachter het totale aantal deeltjes in de kern. Omdat er bij tritium bijvoorbeeld drie deeltjes in de kern zitten, heet dit waterstof-3: 1 proton + 2 neutronen = 3 kerndeeltjes. Chemisch gezien gedragen isotopen van een chemisch element zich bijna hetzelfde, maar ze hebben een verschillende massa en sommige isotopen zijn instabiel, dus radioactief.
Waarom zijn sommige atoomkernen radioactief?
Protonen en neutronen houden elkaar in evenwicht. Protonen voorkomen namelijk dat neutronen uit elkaar vallen: dan verandert een neutron namelijk in een proton en dat is energetisch gezien ongunstig, als er al een ander proton in de buurt zit. Protonen stoten elkaar namelijk af omdat ze dezelfde, positieve elektrische lading hebben. Neutronen zijn de lijm die protonen aan elkaar laten plakken.
Dus als het aantal protonen en neutronen te veel van elkaar verschilt, wordt een atoomkern instabiel. (Dit klopt voor 99%. Het zit iets ingewikkelder. Zo zijn er ook magische getallen en zware atoomkernen hebben meer neutronen nodig als lijm om stabiel te blijven. Maar waarschijnlijk zit je als lezer niet te wachten op een college kernfysica).
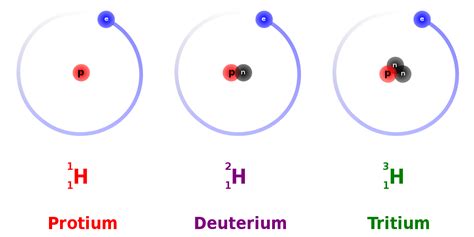
Protium, deuterium en tritium
Bijna alle waterstofatomen hebben alleen een proton in de atoomkern. Deze isotoop, waterstof-1, heet met een deftig woord protium. Ongeveer een op de 30.000 waterstofatomen heeft ook een neutron in de kern. Deze isotoop, waterstof-2, staat bekend als deuterium. Als je ergens op een gezondheidswebsite deuteriumarm water voorbij ziet komen, dan weet je dus nu wat er bedoeld wordt: water waarin alleen protium voorkomt. Sommige gezondheidgoeroes geloven dat ook een beetje deuterium slecht is voor de gezondheid.
Protium en deuterium zijn stabiel. De waterstofisotoop tritium, waterstof-3, heeft behalve het proton, twee neutronen in de kern. Dat maakt de atoomkern van tritium instabiel en daarmee radioactief. Want in ongeveer 12 jaar valt de helft van het tritium uit elkaar in helium-3 en een elektron. Daarbij komt een beetje energie vrij, rond de 5,6 keV. Helium-3, met twee protonen en een neutron in de kern, is stabiel.
Het probleem van een miljard liter water
Na de kernramp in Fukushima was de directe omgeving van de reactor radioactief vervuild. Om te voorkomen dat de omgeving nog verder besmet werd, sloegen de Japanners alle water dat weg lekte uit de omgeving van deze reactor op. Op chemische wijze kan je alle isotopen behalve tritium verwijderen uit water en dat hebben de Japanners ook gedaan. Met tritium kan dat niet. Immers, tritium is chemisch gezien waterstof: dezelfde waterstof (H) die ook in water (H2O) zit.
Ondertussen is dit uitgegroeid tot een kleine miljard liter water, een kubus van 100 x 100 x 100 m. Hierin zet in totaal omgerekend rond de 3 g tritium. Als je dat met zuurstof verbindt, krijg je een half borrelglaasje tritiumwater. Er is op het terrein rond de centrale geen plaats meer om dit water op te slaan. Daarom willen de Japanners het water verdunnen en met het oceaanwater mengen. Oceaanwater beval ook tritium, maar dit is per liter duizend keer zo weinig als het Fukushimawater.

Hoe gevaarlijk is tritium?
Tritium is één van de minst gevaarlijke radioactieve isotopen. Tritium verdwijnt binnen enkele dagen tot weken uit het lichaam. Als er een tritiumkern uit elkaar valt, komt er een elektron met ongeveer 5600 elektronvolt aan energie vrij. Dat is veel minder dan de optater die de elektronen in een ouderwetse beeldbuistelevisie krijgen: rond de 30.000 elektronvolt of meer. Het zwervende elektron raakt snel zijn energie kwijt zonder schade aan te richten, omdat elektronen erg licht zijn.
Als een radiumkern explodeert, is dat driehonderd maal zo veel. En tot overmaat van ramp hoopt radium zich in de botten op.
Het voornaamste probleem zit hem in de vorming van vrije radicalen. Dat zijn groepjes atomen met een ontbrekende plek. Als een tritiumatoom in helium verandert, verdwijnt er namelijk een waterstofatoom. En als dat waterstofatoom toevallig in DNA zit, kan dat een mutatie opleveren. Dit is dan ook waar sommige mensen bang voor zijn.
Nu wil het geval dat er van nature al behoorlijk wat tritium wordt gevormd, door kosmische straling. Per jaar is dat wereldwijd ongeveer dertig kilo. In de oceanen zitten honderden kilos. Dus alle tritium in het water van Fukushima staat gelijk met minder dan een paar uur natuurlijke tritiumproductie. Ons lichaam is goed voorbereid op het repareren van schade, met speciale enzymen, zolang de hoeveelheid beschadigingen laag blijft. Want we leven al in een behoorlijk radioactieve omgeving.

Duizend keer verdund
In principe zou het water van de Fukushima-opslag dus, flink verdund, gemengd kunnen worden met het oceaanwater. Daarmee zou het oceaanwater dan binnen de natuurlijke variatie tritium bevatten. Flink verdund, bijvoorbeeld duizend maal of meer, daalt de radioactiviteit tot rond het natuurlijke niveau. Dus kunnen zeedieren en ook mensen zonder waarneembare gevolgen de uiterst beperkte radioactieve schade verdragen.
Wat dat betreft, zijn bijvoorbeeld dingen als zwerfplastic, of giftige rookwolken van fossiele elektriciteitscentrales, duizenden malen schadelijker voor het oceaanleven en ook voor de mens. Organisaties als Greenpeace die zich nu fel verzetten tegen deze onschadelijke lozing, kunnen zich beter druk maken om echt grote milieuproblemen als zwerfplastic, kolencentrales, loodaccu’s en de zeer smerige uitstoot van vrachtschepen.


